De chemie kan niet zonder formules. Zo veel mogelijk proberen wij het verhaal van de strijd tussen chemie en bacterie in woorden over te brengen; met af en toe een verhelderend plaatje. Deze aflevering staat bol van de formules, met centraal de beta lactam structuur. U kunt de aflevering overslaan of toch maar lezen en de formules laten voor wat ze zijn.
Project ‘100 jaar antibiotica’
Aflevering 22. ‘America First’
Aflevering 23. Ere wie ere toekomt?
Aflevering 24. Chemische formules
Aflevering 25. Omzien en doorgaan
Aflevering 26. Ontwikkeling van penicilline buiten VS en VK
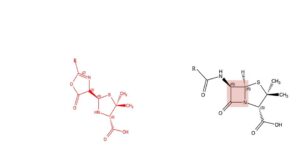
Een relatief klein molecuul
Rond de formule voor penicilline is op hoog niveau strijd geleverd, met bijna uitsluitend Nobelprijswinnaars als spelers. Het dispuut speelt zich af tussen 1940 en 1949. Ernst Chain (Nobelprijs 1945) van het Oxford team doet het meeste voorbereidende werk en stelt vast dat penicilline geen enzym of eiwit kan zijn. Hij denkt aan een relatief klein molecuul met de elementen koolstof (C), waterstof (H), stikstof (N) en zuurstof (O). Tot veler verrassing blijkt er ook zwavel (S) in te zitten. Samen met Edward Abraham stelt hij in 1943 een bèta-lactam structuur gefuseerd met een vijfring voor. De formule rechts, in zwart. De groep R kan verschillend van aard zijn, waarover later meer. De vierring, in het gekleurde vlak, is nogal onverwacht. Het is een zogenaamd beta-lactam en tot dan toe is zo’n structuur nagenoeg onbekend. Bovendien verwacht men dat zulke stoffen weinig stabiel zijn en niet boven 00C kunnen bestaan. Dat de natuur, een schimmel nota bene, zoiets kan maken – dat kan toch niet waar zijn. Robert Woodward (Nobelprijs 1965) is ervan overtuigd dat zoiets wel kan. Twee andere Nobelprijswinnaars, Robert Robinson (Nobelprijs 1947) en John Cornforth (Nobelprijs 1975), kunnen het zich niet voorstellen en stellen een andere structuur voor; de rode formule links. Over de rechterkant van de structuur, de thiazolidine vijfring, zijn ze het eens. Voor de onwaarschijnlijke bèta-lactam 4-ring hebben ze de stabiele oxazolon 5-ring bedacht.
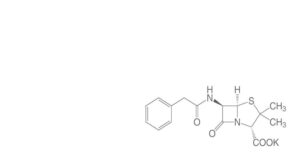
Er moet een andere Nobelprijswinnaar aan te pas komen om het pleit te beslechten. Daarvoor moet Chain wel eerst zeer zuivere en kristallijne penicilline leveren. Samen met Dorothy Crowfoot Hodgkin slaagt hij erin nette kristallen van het natrium-, kalium- en rubidiumzout van Penicilline G te krijgen (zie formule hiernaast). De X-stralen foto van deze kristallen geeft in 1945 het definitieve antwoord: penicilline bevat de bèta-lactam ring gefuseerd met de 5-ring. Het is het grootste organische molecuul waarvan tot dan toe met X-ray- en Röntgenopnames de structuur is vastgesteld. Maar penicilline is aan het eind van WO II nagenoeg staatsgeheim, en pas in 1949 wordt een en ander voluit gepubliceerd. Dat geeft Robinson de gelegenheid zijn foutieve structuurvoorstel nog een paar jaar vol te houden. Dorothy Hodgkin krijgt in 1964 de Nobelprijs. Margaret Thatcher, die bij Hodgkin heeft gestudeerd, heeft later als bewijs van wat vrouwen kunnen bereiken, haar portret op haar werkkamer hangen.
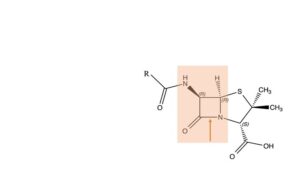
Grote stappen
Nu, 75 jaar later, weten tot op het atoom nauwkeurig hoe het allemaal in zijn werk gaat. Hoe en waarom de schimmel uit drie aminozuren, L-α-amino-adipinezuur, L-cysteïne en L-valine, het penicillineskelet in elkaar zet. We weten waar op het DNA van de schimmel de codes voor deze aminozuren liggen; en ook de codes voor de enzymen die de drie aminozuren aanzetten tot de vorming van het penicillinemolecuul. Afhankelijk van de soort schimmel is de groep R verschillend van structuur. We weten op welke plek penicilline de bacterie aanpakt en hoe de bacterie stap voor stap het loodje legt. We weten welk arsenaal aan verdedigingsmiddelen de bacterie heeft of aanmaakt, en hoe hij die inzet. Hoofdrolspeler in beide processen is de beta-lactam binding, aangegeven met de rode pijl. Bij de aanval van penicilline op bacterie gaat deze binding open en hechten de uiteinden zich aan de celwand van de bacterie. Zodanig dat de celwand lek wordt geprikt en de bacterie zijn levenssappen kwijt raakt. Maar resistente bacteriën pakken precies diezelfde bèta-lactam binding aan; met behulp van een enzym dat ze hebben leren aanmaken. En wel voordat het penicilline zijn schadelijke werk aan de celwand kan afmaken. Bij de bespreking van Clamoxil (Augmentin), een combinatie van Amoxicilline en Clavulaanzuur, zullen we laten zien hoe de wetenschap daar weer een antwoord op heeft gevonden.
Ontwikkeling van bèta-lactam antibiotica
In dezelfde strijd tegen resistentie en infectie hebben chemici alles veranderd aan het penicillinemolecuul wat men zich maar kan voorstellen. Ook de natuur doet hier volop in mee! Alles lijkt geoorloofd, maar één onderdeel van de structuur blijft steeds intact: de bèta-lactam 4-ring (het rode vlak in de formule). In de loop van de tijd zetten onderzoekers een aantal grote stappen in de ontwikkeling van bèta-lactam antibiotica. Niet helemaal in chronologische volgorde zijn dat de volgende.
De groep R, waarop de natuur ook al variaties toepast, is door tientallen groepen vervangen; daaruit ontstaan de bekende semisynthetische penicillines. De twee verreweg belangrijkste vertegenwoordigers, Ampicilline en Amoxicilline zullen we later in meer detail bespreken. De meest bekende natuurlijke penicillines zijn PenG en PenV.
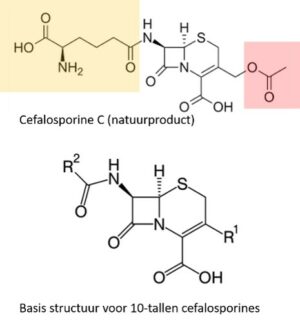
In een riool op Sardinië ontdekt men in 1948 de Cefalosporine schimmel en dit opent een nieuw speelveld. In 1958 stellen Edward Abraham en Dorothy Hodgkin de structuur vast: de natuur heeft de 5-ring in penicilline vervangen door een 6-ring. De bacteriën die hadden geleerd de beta-lactam binding in penicilline te verbreken worden alsnog te grazen genomen, want de 6-ring zorgt ervoor dat het resistentie-enzym de beta-lactam binding in de cefalosporines niet beet kan pakken. Door vervanging van de twee zijketens (gekleurd aangegeven in het natuurlijke Cefalosporine C) door een schier eindeloze variatie aan andere groepen (R1 en R2) ontstaan tientallen nieuwe semisynthetische anti-infectie middelen. Bekende namen zijn Cefalexine, Cefadroxil, Cefachlor, Cefamandol, Cefixime en Cefotaxime.
We hebben nooit de natuur kunnen verslaan met een goedkope synthese van penicilline in het laboratorium, ondanks heel veel werk. Misschien voelden onderzoekers zich uitgedaagd doordat wij de sulfa’s eenvoudig synthetisch kunnen maken. Zeker in de beginjaren durft een aantal fabrikanten de sprong naar de lastige fermentatie niet aan, in de overtuiging dat er in de nabije toekomst een eenvoudige synthese gevonden zal worden. De beta-lactam 4-ring is inderdaad synthetisch te doen, maar alle processen zijn in de praktijk veel te duur. De grootste strijder op dit punt is de Amerikaanse chemicus John Sheehan. Hij weet het natuurlijke PenV in het lab te maken. Maar elke labsynthese van de 3-amino-bèta-lactamring is een wetenschappelijke curiositeit gebleven zonder enige commerciële potentie.
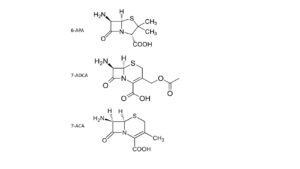
Het inzicht in de werkwijze van de natuur groeit zeer snel; daarmee groeit ook de kans op een betere biosynthese. Men slaagt er al snel in, de genetische informatie voor de biosynthese van penicilline over te brengen in gistcellen; deze produceren vervolgens goed en goedkoop veel penicilline. Het werk van Sheehan leidt er wel toe dat de industrie de beschikking krijgt over drie belangrijke bouwstenen voor vrijwel alle penicillines en cefalosporines: 6-APA, 7-ACA en 7-ADCA. Alle drie stoffen hebben direct of indirect de natuurproducten Penicilline G of Cefalosporine C als basisgrondstof. Ze zijn stabieler en beter houdbaar dan de meeste eindproducten, vanwege hun aminozuurkarakter (en stabilisatie als Zwitter ion).
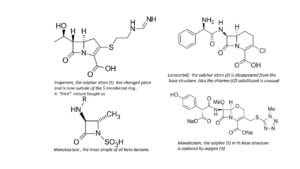
Bij de ontwikkeling van de bèta-lactam antibiotica blijft tientallen jaren de 5-ring (in de pen’s) of de 6-ring (in de cef’s) onaangetast. Maar toenemende resistentie leidt eind vorige eeuw tot een enorme stroom nieuwe moleculen. Alleen de bèta-lactam 4-ring blijft intact. Het leidt ook tot het eenvoudigste product, monobactam, een stof met beperkt klinisch succes; en tot heel ingewikkelde structuren met grote zijgroepen. Sommige stoffen hebben klinisch succes zoals Loracarbef, Moxalactam en Imipenem. De laatste stof is weer afgeleid van het natuurproduct Thienamycine; in de formule daarvan laat de natuur opnieuw een variant op het penicillinemotief zien.
