Het succes van de penicillines lokt een grote zoektocht uit naar micro-organismen met antibacteriële werking. Zijn er beter producerende schimmelstammen te vinden? Ja, die zijn er. Zo ontdekt de Italiaan Guiseppe Brotzu in 1948 in een rioolpijp aan de kust van Sardinië de schimmel Cephalosporium Acremonium. Het ruwe filtraat blijkt de beruchte Staphyllococcus Aureus de baas te kunnen zijn. Het bevat cefalosporines, een natuurlijke variatie op het penicilline motief. De bron van een grote reeks succesvolle antibiotica met brede toepassing, tot op de dag van vandaag.
Project ‘100 jaar antibiotica’
Aflevering 28. Het succes van Bacinol
Aflevering 29. De Gist; van illegaal naar wereldspeler
Aflevering 30. Cefalosporines
Aflevering 31. Hulp uit onverwachte hoek
Aflevering 32. Keerpunt 1950

Lessen geleerd
Edward Abraham van de bekende penicillinegroep in Oxford gaat direct met de nieuwe schimmel aan de slag. Succes neemt ook hier weer zijn tijd. Tien jaar later, tijdens een skivakantie, weet hij zeker wat de structuurformule moet zijn; en de bekende Dorothy Hodgkin bevestigt weer zijn gelijk. Ook lukt het Abraham het cefalosporinemolecuul iets aan te passen tot een zeer goed bruikbaar geneesmiddel. Na alle lessen uit het penicillineverleden vraagt Abraham nu wel octrooi aan. De Amerikaanse firma Eli Lilly brengt in 1964 het eerste succesvolle semisynthetische cefalosporine, cefalotin, op de markt. De royalty’s lopen binnen bij Abraham en hij wordt er een rijk man mee. Maar het meeste geld gaat naar drie stichtingen voor bevordering van onderzoek in een brede context. Op dit moment beschikken ze over ca. 200 miljoen pond. De Universiteit van Oxford heeft in de loop der jaren tientallen miljoenen ontvangen, onder meer voor de bouw van laboratoria en congrescentra. Ook hebben veel studenten een beurs gekregen uit één van de fondsen.

Zoals gemeld in aflevering 23 leidt het werk van Abraham en collega’s uiteindelijk tot drie bouwstenen, 6-APA, 7-ACA en 7-ADCA. Hieruit komt een grote reeks succesvolle medicijnen voort: de semisynthetische penicillines (SSP’s) en cefalosporines (SSC’s). We zijn inmiddels bij de vijfde generatie cefalosporines beland.
Cefalosporines, hoe werken ze ook al weer
Het werkingsmechanisme van de SSC’s en SSP’s is bijna altijd hetzelfde. Populair gezegd prikken deze stoffen de celwand van de te bestrijden bacterie lek. Die loopt leeg, kan zich niet vermenigvuldigen en sterft. Nu weten we tot op elke moleculaire stap nauwkeurig hoe dat in zijn werk gaat. Het spel speelt zich af aan de buitenkant van de bacterie. Een groeiende bacterie (vooral aanwezig bij een verse infectie) moet zijn celwand voortdurend uitbouwen. Dat gebeurt door de bouwstoffen vanuit de cel naar de buitenkant te brengen, door de groeiende celwand heen, en daar te assembleren tot nieuwe wanddelen. Eén van de enzymen die twee belangrijke onderdelen aan elkaar koppelt heeft ook een goede bindingsplaats voor een SSC of SSP op de plek waar het metselwerk plaats vindt. Maar eenmaal op zijn plaats, blijft het SSC of SSP stevig op die plek waardoor het bouwen stil valt. Het geheime wapen is daarbij de beta-lactam binding in het SSC/P. Die wordt open geknipt door een onderdeel van het bovengenoemde enzym en de losse einden binden zich links en rechts aan het enzym.
Resistentie
Het geheime wapen teniet doen is natuurlijk de meest voor de hand liggende manier voor de bacterie om de werking van het antibioticum te saboteren. In zijn algemeenheid zijn er ook andere werkwijzen. Zo kan de bacterie kleine veranderingen in zijn celwand aanbrengen waardoor het aanknopingspunt voor het antibioticum verdwijnt. Ook zijn er mechanismes waarbij de bacterie de binnendringers zo snel mogelijk weer naar buiten pompt.
In het geval van de penicillines en de cefalosporines berust resistentie vrijwel altijd op de actie van een zogeheten bèta-lactamase enzym; een enzym dat de cruciale bèta-lactam binding open knipt. Al doende (in de loop van vele mutaties) hebben de meeste ziekteverwekkende bacteriën zo’n enzym ontwikkeld. En daarbij heeft de resistente bacterie er wel voor gezorgd dat het lactamase enzym de losgeknipte onderdelen direct weer los laat, zodat het een volgend molecuul aan kan pakken. De slimste bacteriën sturen hun lactamases al door hun celwand naar buiten als een SSC of SSP in de buurt komt.
Een strijd zonder eind
Tot nu toe kon men misschien denken dat wij juichend verslag hebben gedaan van de 100-jarige strijd tussen chemie en bacterie. Vanaf nu zullen we het er steeds vaker over hebben dat er geen overwinnaar in zicht is. Op dit moment is de stemming somber; we worden weer bang voor dodelijke infecties. Toch zijn die bedreigingen bij lange na niet van het niveau dat onze (over)grootouders onder ogen moesten zien. We hebben een groot arsenaal aan middelen ter beschikking en de meeste patiënten zijn (nog) niet in aanraking geweest met resistente bacteriën. Maar men verwacht miljoenen slachtoffers door resistentie in 2050 en daar worden we behoorlijk zenuwachtig van.
De ontwikkeling van steeds weer nieuwe varianten van bestaande middelen heeft ons lange tijd op voorsprong gezet. De slimste daarvan zullen we hier beschrijven. Ze berusten allemaal op het foppen van het lactamase enzym dat de resistente bacterie gebruikt om zijn belager af te weren. Het kan daarbij gaan om het aan elkaar zetten van twee bekende antibiotica; bij voorbeeld een SSC of SSP en een erythromycine. De resistente bacterie valt het SSC of P aan en schakelt het uit; maar dan is het erythromycine al binnen om zijn werk te doen. Andere methodes maken gebruik van twee verschillende bèta-lactam producten waarbij het lactamase van de bacterie een duidelijke voorkeur heeft voor één van beide.
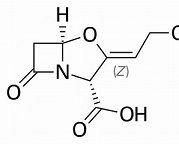
Clavulaanzuur
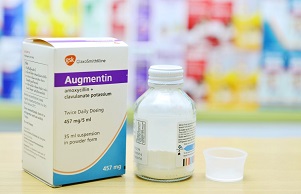
Bij het meest succesvolle voorbeeld wordt het antibioticum gecombineerd met clavulaanzuur. Dit heeft de bruikbaarheid van de meest succesvolle SSP, amoxicilline, met enkele tientallen jaren verlengd. Een succes dat nog volop gaande is. Door de combinatie met clavulaanzuur wordt het lactamase van de resistente bacterie om de tuin geleid. Clavulaanzuur heeft zelf geen antibiotische werking, maar het bevat wel een bèta-lactam binding, en het lactamase van de resistente bacterie heeft daar een grote voorkeur voor. Amoxicilline kan vervolgens zijn werk doen als van ouds. Augmentin is één van de merknamen waarmee de combinatie op de markt is. Dit is een vinding van de Engelse firma Beecham uit de jaren ‘70 en ‘80 van de vorige eeuw. Clavulaanzuur is overigens niet het werk van slimme chemie; het wordt geproduceerd door een streptomycinestam en lijkt dus eerder onderdeel van het wapenarsenaal waarmee micro-organismen elkaar naar het leven staan. Clavulaanzuur werkt ook in combinatie met andere SSC’s of SSP’s, maar de combi met Amox is verreweg het meest populair.
Op de veterinaire markt is deze combinatie ook in gebruik. Hij wordt toegepast bij honden, katten, runderen en varkens. In combinatie met prednison is de combinatie in gebruik bij het droogzetten van drachtige koeien en het bestrijden van uierontsteking. Gebruik in veevoer is steeds meer verboden of omstreden. Want om de hoge efficiency van Augmentin voor humaan gebruik zo lang mogelijk te behouden zal de veterinaire sector toch moeten gaan omzien naar alternatieven.
Geraadpleegde bronnen:
Wikipedia: alle genoemde eigennamen en producten
The Mould in Dr Florey’s Coat. Eric Lax, Abacus 2004. ISBN 978-0349-11768-3
Antibiotics: from prehistory to the present day, Kate Gould, Journal of Antimicrobial Chemotherapy 71, 572-575(2016)
N0-nonsense Guide to Antibiotics, Moira Dolan, SmartMedInfo, 2015; ISBN: 978-09968860-2-4
History and Current Use of Antimicrobial Drugs in Veterinary Medicine, John F Prescott, Microbiol. Spectr. 2017
